1. 실험 제목 : PDMS를 이용한 미세접촉 인쇄
2. 실험 날짜 :
3. 실험 목적 :
PDMS 고무를 이용하여 자기 조립 단분자막의 미세접촉 (microcontact) 전사 실험을 수행한다.
4. 실험 이론 :
이 실험에서는 유기 금속 반응을 통해 가교되는 투명 고무인 PDMS를 도장으로 사용하는 미세접촉 인쇄 실험을 수행한다. 동전 모양대로 성형된 PDMS의 소수성 표면에 소수성인 알케인싸이올(alkanethiol)을 묻힌 후 은 표면에 알케인싸이올을 전이시키면 도장 모양대로 친수성, 소수성 표면이 형성된다. 이때 알케인 싸이올과 은 사이에 다음과 같은 반응이 일어나 매우 안정한 결합이 형성되며 알케인 싸이올들의 긴 소수성 사슬들은 분자 간 상호작용(분산력)에 의해 매우 조밀하게 자기 조립 (self-assembly) 되어 소수성 표면 형성 반응의 또 다른 원동력으로 작용한다.

친수성과 소수성이 공존하는 표면에 수증기를 응축시키면 친수성 표면에만 선택적으로 수증기가 응축되어 도장의 모양이 구분될 수 있다.
PDMs는 alkanethiol과 같은 유기 물질이 매우 균일하게 코팅될 수 있는 소수성 표면을 가지고 있으며, 수백nm이하의 매우 작은 선폭으로 원하는 모양을 기질 표면 위로 인쇄할 수 있으며, 도장을 여러 번 반복하여 재사용할 수 있으므로 미세 접촉 인쇄는 반도체 공정 등의 공정 비용을 절감할 수 있는 획기적인 방법으로 각광받고 있다.
*미세접촉인쇄(microcontact printing) 과정
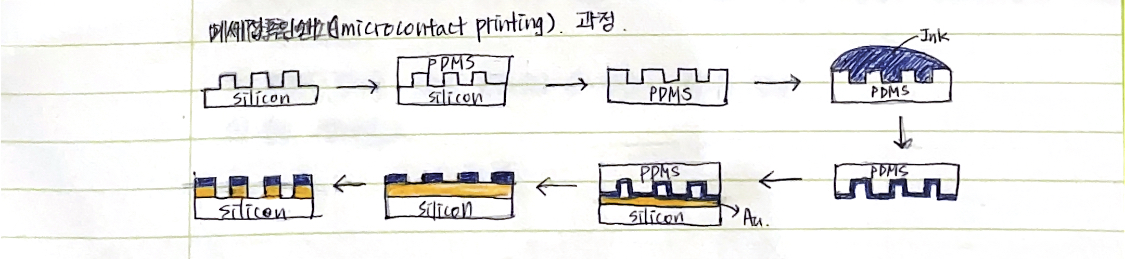
*자기조립 단분자막(SAM)
자기조립단분자막(SAM)은 고체 표면에 자발적으로 형성되는 유기 단분자막을 말한다.

5. 시약 및 기구 :
0.5M 글루코스 (0.90g glucose를 10ml 물에 녹임)
0.8M KOH (0.45 KOH를 10ml 물에 녹임)
0.1M 질산은 (0.17g AgNO3)를 10ml 물에 녹임)
15M 진한 수산화 암모늄 (진한 암모니아수를 희석하지 않고 사용)
페트리 접시
현미경 슬라이드
PDMS 염기와 경화제 (Dow corning Sylgard Elastomer 184 Kit)
Weighning boats (100ml)
Stir sticks
금형 (작은 알루미늄 웨잉보트로 대체가능)
오븐 (120'c)
알케인싸이올 용액 (몇 방울의 긴사슬 알케인싸이올을 20ml 에탄올에 녹임)
(알케인 싸이올: 알케인에 sulfhydryl기 (-SH)를 가진 화합물)
6. 실험 방법 :
- 슬라이드 글라스에 은코팅 하기
1) 10ml의 0.1M 질산은 (silver mitrate)(AgNO3)에 수산화암모늄(ammonium hydroxide)(KOH)을 몇 방울 떨어뜨려서 검게 생긴 침전물이 녹도록 한다.
2) 5ml의 0.8M KOH를 더한다. 검은 빛깔의 침전물이 생긴다.
3) 수산화 암모늄을 떨어뜨려 검게 생긴 침전물을 녹인다. -> 활성은 용액 (active silver solution)
4) 페트리 접시에 유리 슬라이드를 놓고 0.5M 글루코스 용액 12방울, 활성은 용액 40방울을 떨어뜨린다.
5) 페트리 접시를 살살 흔들어서 은 코팅이 되도록 한다.
6) 물로 씻어낸다.
- PDMS 도장 만들기
1) 8.00g의 sylgard 고분자 염기에 0.80g의 경화제 (curing agent)를 더한다.
2) 얇은 나무 막대 (면봉 이용)로 충분히 섞는다.
3) 음파파쇄 (sonication)을 통해 기포를 제거한다. (6-7분)
4) 동전을 넣어둔 은박컵에 PDMS를 부어 넣는다.
5) 121'c 오븐에서 20분 동안 열을 가한다.
6) 실온에서 식히고 PDMS에서 동전을 제고, 도장 가장자리를 따라 절단한다.
- PDMS 도장에 알케인 싸이올 잉크 묻히기
1) 알케인싸이올 에탄올 용액으로 PDMS 위를 완전히 덮는다.
2) 1분 후 에탄올로 도장을 씻어낸다.
3) 상온에 두어 에탄올이 증발하도록 한다.
4) 은 코팅된 슬라이드에 도장을 찍는다. (살며시 도장을 접촉시키고 약 10초 후 조심스럽게 떼어낸다)
5) 도장 찍은 표면에 숨을 불어 동전의 그림 모양이 나타나는 것을 관찰한다.
7. 참고문헌 :
일반화학실험 (자유아카데미)-p61,p62,p63
Microcontact Printing:Limitations and Achievements (저자 : David N.Reinhoudt, Jurriaan Huskens)
자기조립단분자막을 이용한 표면처리기술 (저자 : 지영석, 강성민, 최인성)
8. 실험 결과 및 고찰 :
몰농도란 용액의 리터당 용질의 몰수를 말한다. (M, molarity, molarconcentration)

몰랄농도(m)란 용매 1kg (1000g)에 녹아있는 용질의 몰수

노르말 농도란 용액 1L 속에 들어있는 용질의 g 당량수

문제:
1) AgNO3 (169.87g/mol) 0.1M, 10ml 만드는데 필요한 양 (g)
2) Glucose (180.16g/mol) 0.5M, 200ml 만드는데 필요한 양 (g)
3) KOH (56.115g/mol) 0.8M, 100ml 만드는데 필요한 양 (g)

*실험에서 AgNO3, KOH, Glucose의 역할
- 질산은 수용액은 암모니아수와 반응하여 앙금을 생성한다.
질산은 수용액에 암모니아수를 넣으면

착이온이 형성된다. 착이온이란 중심에 있는 전이금속의 양이온에 몇 개의 분자 또는 이온이 결합되어 있는 물질 속에서 중심원자에 결합되어 있는 이온으로 둘러싸인 금속 이온으로 이루어진 전하를 띠는 화학종을 말한다.
- 글루코스는 은이온을 은으로 환원시키는 역할을 한다.
글루코스 끝부분에 존재하는 포르말기(-CHO)는 환원력이 크기 때문에 환원성이 좋다. 그렇기 때문에 글루코스가 이전에 생성된 착이온을 환원시켜 은이 석출 됨.
- KOH는 환원이 잘 일어나기 우한 촉매이다. 강한 염기성을 띄고 있다.
2AgNO3 + 2KOH -> Ag2O + 2KNO3 + H2O
실험상 생기는 아세틸 결합을 가수분해하는 역할이다.
도움이 되셨다면 공감이나 댓글 부탁드립니다.✒️
제 블로그를 찾아주셔서 감사합니다!
'실험노트 > 일반화학 실험' 카테고리의 다른 글
| [실험노트] 일반화학 실험 7. 비누화 반응 (2) | 2023.11.17 |
|---|---|
| [실험노트] 일반화학 실험 6. 카페인 추출 (0) | 2023.04.29 |
| [실험노트] 일반화학 실험 4. PDMS 탱탱공 만들기 (0) | 2022.09.02 |
| [실험노트] 일반화학 실험 3. 크로마토그래피 (1) | 2022.08.31 |
| [실험노트] 일반화학 실험 2. 몰 질량의 측정 (0) | 2022.08.30 |




댓글