1. 실험 제목
: 크로마토그래피
2. 실험 목적
: 정상 크로마토그래피와 역상 크로마토그래피에 의한 색소의 분리를 통하여 크로마토그래피의 원리와 극성의 개념을 배운다.
3. 실험 이론
: 혼합물을 구성하는 화합물의 종류와 용도를 알아내는 방법은 다양하지만 대부분의 방법에서 혼합물을 각각의 상분으로 분리하는 것은 분석의 필수적인 중간과정이 된다. 크로마토그래피는 최근에 가장 많이 사용하는 분리 방법의 하나이다.
크로마토그래피란 적절한 정지상과 이동상을 사용하여 시료들이 섞여 있는 혼합물을 이동 속도 차이를 이용하여 분리하는 방법이다. 예를 들어 검은 수성 사인펜으로 글씨를 쓴 종이를 물에 담그면 번진 부분은 푸른색, 빨간색, 노란색 등의 색깔로 퍼지게 된다. 이것이 각 색소의 이동 속도가 다르기 때문에 나타나는 현상이다.
크로마토그래피에는 화합물이 고체 표면에 흡착되는 정도의 차이를 이용한 '흡착 크로마토그래피', 작은 분자가 교대로 결합된 겔의 틈새를 잘 침투하는 효과를 이용하는 '겔 투과 크로마토그래피', 주어진 pH에서 화합물이 해리해서 생긴 이온의 전하 차이를 이용하는 '이온 교환 크로마토그래피', 용매에 녹는 정도가 다른 점을 이용한 '분배 크로마토그래피' 등의 방법이 있다. 이 실험에서는 분배 크로마토그래피를 다루기로 한다.
예를 들어, 석유에터와 물 혼합용액에 분자의 극성이 다른 설탕, 아세트산, 식용유를 넣고 흔들어준 후 두 층으로 갈라지게 하면 극성이 큰 설탕은 대부분 극성이 큰 물에 녹아있고 극성이 작은 식용유는 극성이 작은 석유에터에 녹아있게 된다. 물 보다 극성이 작은 아세트산은 물과 석유 에터층에 비슷하게 분배된다. 이와 같이 물질마다 두 가지 용매에 대한 분배 계수가 다른 점을 이용하는 크로마토그래피를 '분배 크로마토그래피'라고 한다. 고체 표면에 얇은 액체의 막을 입힌 정지상 사이로 극성이 다른 용액 (이동상)을 흘려주면서 두 액체 사이에 물질의 분배가 일어나도록 하는 경우를 액체-액체 분배 크로마토그래피라고 하고 기체를 이동상으로 이용하는 경우를 기체-액체- 분배 크로마토그래피라고 한다.
정상:
처음에는 실리카겔이나 알루미나 같이 극성이 큰 고체 표면에 물 같이 극성이 큰 액체 막을 입힌 정지상과 극성이 작은 용액을 이동상으로 사용하는 정상 액체 크로마토그래피 방법이 개발되었다. 실리카겔의 얇은 막을 알루미늄이나 플라스틱 판에 입힌 정지상을 사용하는 얇은층 크로마토그래피를 이용해서 색소를 분리한다. TLC에서의 이동상은 보통 전개제라고 부르며, 뷰탄올, 아세트산, 암모니아처럼 물 보다 극성이 작은 화합물의 혼합용액이 많이 사용된다. 모세관 현상으로 전개제가 TLC관 위쪽으로 전개될 때 시료 분자들도 함께 퍼지게 되는데, 시료 분자들이 정지상에서 노출된 실리카겔의 실란올기와 이동상 사이에 분배되는 계수가 다르기 때문에 전개제가 위쪽으로 올라가면서 시료 분자들이 분리된다. 각 시료가 움직인 거리와 용매가 움직인 위치 (용매선)까지의 거리의 비를 'R+값'이라 하며, 이 값은 화합물과 사용하는 전개제의 종류에 따라 독특한 값을 나타내기 때문에 물질의 확인에 매우 유용하다.
역상:
역상 액체 크로마토그래피에서는 옥타데실기(-C18H37)처럼 긴 탄화수소 사슬이 공유결합으로 결합된 막을 입힌 작은 입자를 정지상으로 사용한다. 탄소와 수소는 전기 음성도의 차이가 작기 때문에 C-H결합은 비극성이고, 37개의 C-H 결합을 가진 C18기로 된 정지상은 극성이 대단히 낮은 분자 단위의 액체막이라고 생각할 수 있다. 역상 액체 크로마토그래피에서는 물과 유기용매를 섞어서 극성을 조절한 혼합 용액을 이동상으로 사용한다. 극성이 다른 색소의 혼합물을 C18카트리지에 통과시키면 극성이 작은 색소는 C18기와 상호작용을 하기 때문에 정지상에 오래 머물게 되고, 물과 상호작용을 더 잘하는 극성이 큰 화합물은 물을 따라 먼저 흘러나오게 된다.
*정상 크로마토그래피 : 정지상 극성, 이동상 비극성
*역상 크로마토그래피 : 정지상 비극성, 이동상 극성
*모세관 현상: 액체의 응집력, 관과 액체 사이의 부착력에 의한 현상
*이동상 : 분석물을 끌고 가는 매개체. 이동상 종류에 따라 GC/LC로 구분
*정지상 : 분석물을 분리하기 위한 매개체. 보통 column의 충진물을 의미
참고) 분리: seperation. 혼합물을 순물질로 나누는 작업이다. 분리의 방법에는 증류(액체 시료 속의 불순물을 분리하는 수단), 재결정 (고체상태인 혼합물을 분리하는 방법), 추출 (액체 용매를 사용하여 고체 또는 액체에서 어떤 물질을 분리하여 추출하는 조작), 크로마토그래피, 원심분리 (단백질이나 생체 물질의 분리에 이용) 등이 있다.
4. 시약 및 기구
: 500ml 비커, 시계접시, 모세관, TLC 판 (폭 8cm, 높이 6cm), 적색 40호, 황색 5호, 청색 1호 식용색소, 전개제 (1-뷰탄올 : 아세트산: 물 = 60 : 15 : 25) 인 혼합 용액
5. 실험 방법
: 얇은 층 (TLC) 크로마토그래피에 의한 색소의 분리 (정상 크로마토그래피)
1) 적색 40호, 황색5호, 청색 1호의 붉은 혼합용액 각각과 네 가지의 미지 시료를 모세관에 묻혀서 RLC판의 바닥에서 1cm 위치에 1cm 간격으로 일렬로 찍어서 반점을 만들고 말린다.
2) TLC판을 1-뷰탄올 : 아세트산 : 물을 60: 15 : 25 의 비로 혼합한 전개제가 담긴 비커에 넣어서 전개를 시작한다. 시료의 반점이 전개제에 담기지 않도록 TLC판을 수직으로 세우고 시계 접시를 덮어서 전개제가 증발하지 않도록 한다.
3) 전개제가 TLC판의 위쪽 끝에서 1cm 정도 떨어진 곳까지 도달하면 TLC 판을 꺼내서 말리 다음에 Rf 값을 측정한다. 순수한 색소의 Rf 값과 미지 시료의 경우에 생긴 반점들의 R+ 값을 비교해서 미지 시료에 들어있는 색소의 종류를 알아낸다.
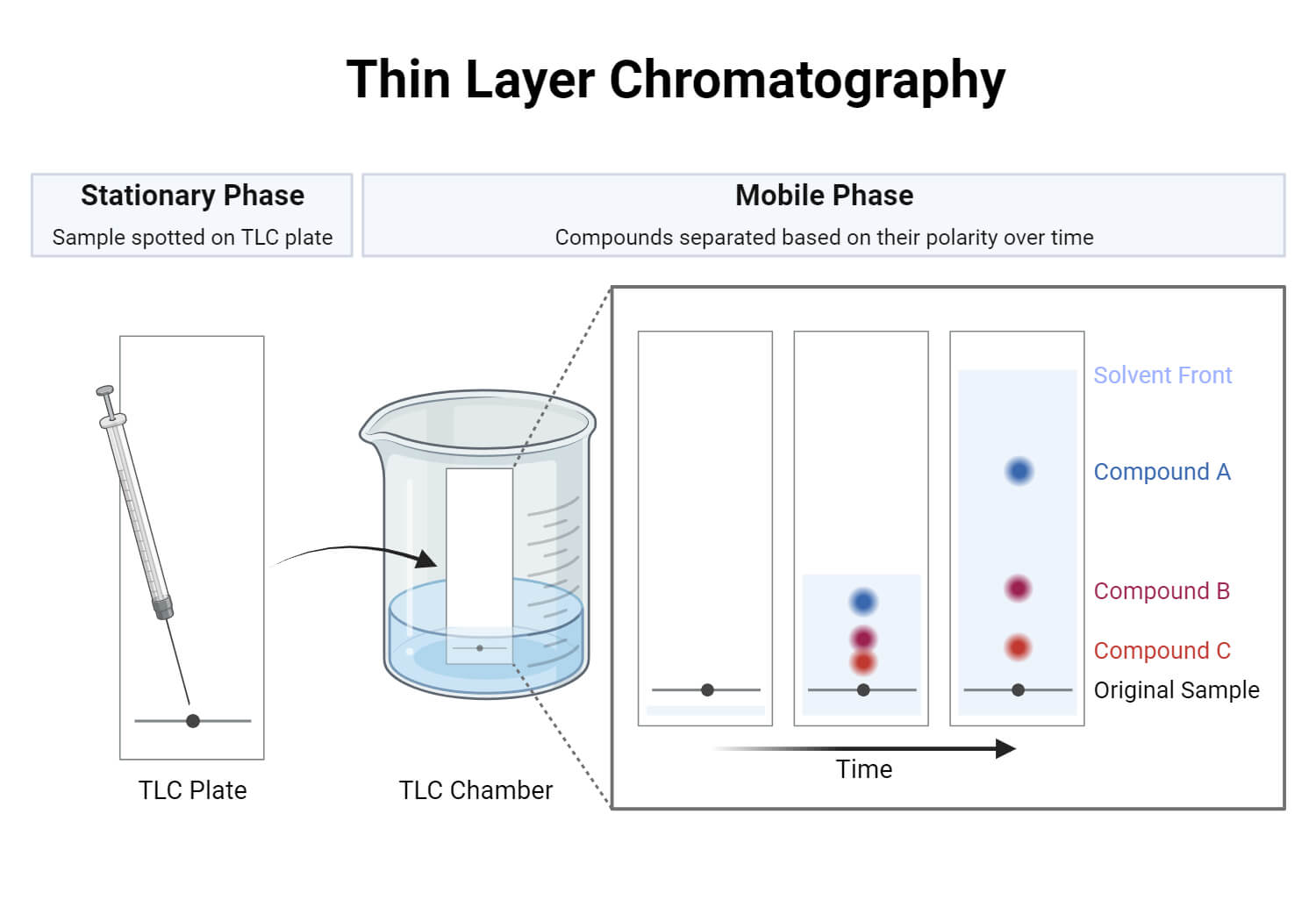
TLC판을 전개액이 담긴 용액에 넣은 모습 -> 시간에 따른 색소의 분리 모습
6. 참고문헌
크로마토그래피(두산백과)
분리(사이언스올)
일반화학실험/자유아카데미
https://microbenotes.com/thin-layer-chromatography/
Thin Layer Chromatography: Principle, Parts, Steps, Uses
Thin Layer Chromatography is the separation or identification of a mixture of components into individual components by using finely divided adsorbent solid / (liquid) spread over a plate and liquid as a mobile phase.
microbenotes.com


7. 고찰
(사진참고)
제 블로그를 찾아주셔서 감사합니다!
도움이 되셨다면 댓글 혹은 공감 부탁드립니다.✒️
'실험노트 > 일반화학 실험' 카테고리의 다른 글
| [실험노트] 일반화학 실험 6. 카페인 추출 (0) | 2023.04.29 |
|---|---|
| [실험노트] 일반화학 실험 5. PDMS 를 이용한 미세접촉 인쇄 (0) | 2023.04.10 |
| [실험노트] 일반화학 실험 4. PDMS 탱탱공 만들기 (0) | 2022.09.02 |
| [실험노트] 일반화학 실험 2. 몰 질량의 측정 (0) | 2022.08.30 |
| [실험노트] 일반화학 실험 1. 아보가드로 수의 결정 (0) | 2022.08.28 |


댓글